Ernährung nimmt eine zentrale Stellung in jedweder Kultur ein. Während diese primär das Überleben der Menschheit sichert und sekundär als Mediator für gesundes Altern wirkt (1), spielt die Ernährung insbesondere im Leben von Sportlern eine entscheidende Rolle. Dabei haben unterschiedliche Teilaspekte des Überbegriffs Ernährung (Energie, Makro- und Mikronährstoffe) natürlich auch unterschiedliche Folgen auf molekularer (DNA-Stabilität), zellulärer (intrazelluläre Signalwege), physiologischer (z.B. Entzündungsreaktionen) und funktionaler Ebene (z.B. Stärke und Kognition).
Wird dies am Beispiel des Fitnesssports festgemacht, so ist es quasi unumgänglich, sich nicht auch mit Ernährung zu beschäftigen: denn Fitness und Ernährung gehen Hand in Hand. Hierbei wird sich der Ernährung als Werkzeug zur Erreichung verschiedenster, fitnessspezifischer Ziele bedient, die die Grundlage für morphologische Adaptationen liefert. So steuert und ergänzt die Ernährung den Trainingsalltag und trägt im Wesentlichen zur Verbesserung von Körperkomposition und Leistungsfähigkeit bei (2). Vorliegend soll spezifisch auf die Rolle zur Veränderung der Körperkomposition durch Gewichtsverlust eingegangen werden, wie dies grundsätzlich bei Übergewicht, aus ästhetischer Perspektive (Bodybuilding) oder aufgrund einer Gewichtsklasse (bspw. Boxen) der Fall sein kann.
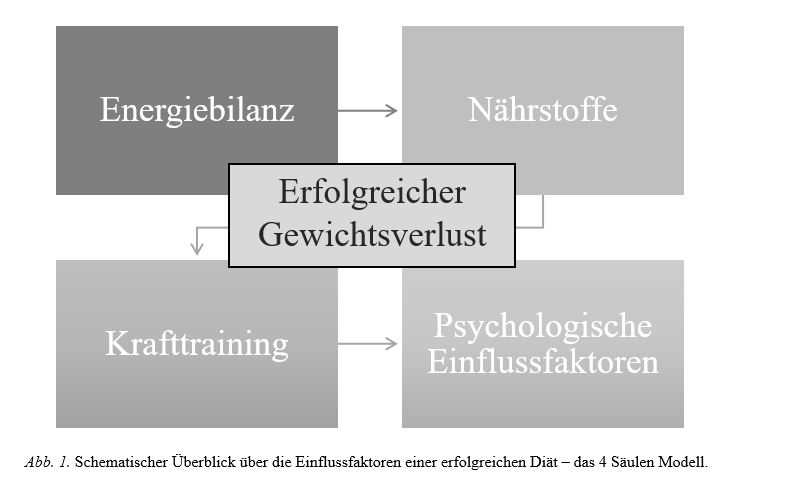
Während dieser Artikel spezifisch auf die Physiologie des Gewichtsverlustes in Perspektive der Energiebilanz eingeht, wird dieser im zweiten Artikel der Reihe durch die Ebene der Nährstoffe (Protein, Kohlenhydrate, Fette sowie Mikronährstoffe) und deren Funktion ergänzt. Im dritten Teil des von uns vertretenen 4 Säulen Modells soll sodann auf die Rolle von Krafttraining (RT) eingegangen werden, welches im letzten Artikel der Reihe um psychologische Hintergründe und Einflussfaktoren im Rahmen des Gewichtsverlustes abgerundet wird. Diese 4 Säulen des Gewichtsverlustes finden sich übersichtsartig in Abb. 1 und sind bewusst nicht, wie üblich, in Pyramidenform dargestellt: Dabei sind sich die Autoren sehr wohl bewusst, dass die Energiebilanz entscheidend für die Abnahme von Körpergewicht ist – eine gesunde und erfolgreiche Diät, ähnlich wie beim Altern, kann jedoch nur durch die Synthese aller Faktoren erfolgen.
Im Zuge dieser ersten Säule wird im Rahmen des Artikels ein kurzer Überblick über den Begriff der Energie und den der derzeit vorherrschenden Modelle gegeben. Im Rahmen des Calories-in Calories-out Modells (CICO) werden kritisch sowohl die Faktoren der Energiezufuhr („in“ Seite) sowie des Energieverbrauchs („out“ Seite) beleuchtet. Hierbei wird sich primär auf den Gewichtsverlust konzentriert und herausgestellt, inwiefern die einzelnen Teilsysteme auf diesen einwirken. Abschließend werden praktische Implikationen für die energetische Ebene entwickelt, die sich hauptsächlich um die Diskussion eines geeigneten Energiedefizits drehen. Sodann sollen mediierende Faktoren aufgezeigt und im Kontext eines bestmöglichen Erhalts von fettfreier Masse reflektiert werden.
Kalorien = Energie?
Seit 1824 wird der Begriff der Kalorie als Einheit für die in der Nahrung enthaltene Energie genutzt, die auch als physikalischer Brennwert bekannt ist (Levine, 2017). Da eine Kilokalorie (kcal) eigentlich 1000 Kalorien (cal) sind, bezieht sich die klassische Aussage „das Essen hat 1000 Kalorien“ genauer gesagt auf die Kilokalorien, definiert als die Energie, die benötigt wird, um 1kg Wasser von 15 auf 16° C zu erhitzen (Buchholz & Schoeller, 2004).
Der Körper ist dabei als (nicht-perfektes) System zu verstehen, der Energie konstant transformiert – nämlich von zugeführter Nahrung zur Produktion von Wärme. Da in diesem Kontext weder Energie erschaffen noch vernichtet wird, ist auch der Körper ein Organismus, der sich den formulierten Gegebenheiten der Thermodynamik beugt (1. Satz der Thermodynamik). Dies wurde bereits Ende des 18. Jahrhunderts bei einem von Lavoisier durchgeführten Experiment an einem Meerschweinchen nachgewiesen (das erste je gebaute Kalorimeter). Im Experiment wurde das Meerschweinchen in einem boxartigen Behälter platziert, der mit Schnee bedeckt war. Der aufgrund der Körpertemperatur schmelzende Schnee wurde aufgefangen und gewogen. Nach 10 Stunden Experiment konkludierte das Forscherteam sodann, dass das Meerschweinchen ca. 30kcal Wärme abgegeben hat (wobei diese vorher berechnet haben, dass zur Schmelzung von 1kg Schnee ca. 80kcal Wärme notwendig waren; Kaiyala & Ramsay, 2011). Da die Nahrungszusammenstellung des Meerschweinchens irrelevant für das Schmelzen des Schnees war, sollte spätestens hier klar sein, dass, aus einer rein thermodynamischen Perspektive, eine Kalorie = Kalorie ist.
Weitergehend wurde aus den Experimenten von Rubner (GER) und Atwater (US) sodann, mit Hilfe von Bomb-Kalorimetern, die Menge an Energie berechnet, die durchschnittlich bei der Verbrennung der Makronährstoffe frei wird (Widdowson, 1955). Die angegebenen Werte (Protein 4.1kcal/g, Kohlenhydrate 4.1kcal/g sowie Fette 9.3kcal/g), auch Atwater-Faktoren genannt, stellen nur gemittelte Werte dar, da die chemischen Eigenschaften der Nährstoffe auch deren Brennwert beeinflussen. Nichtsdestotrotz kann die Energie, die bei der Verbrennung von Nährstoffen in Bomb-Kalorimetern (reine Energie) frei wird, nicht mit der Menge an Energie gleichgesetzt werden, die dem Körper anschließend für physiologische Prozesse zur Verfügung steht. Dies wird u.a. damit begründet, dass der Körper kein perfektes System ist; der ergo nicht alles spalten, was grundsätzlich verbrannt werden könnte. Nicht-spaltbare Anteile der Nährstoffe werden schließlich mit Urin und Fäzes ausgeschieden. Hieraus wurde schließlich das Konzept der metabolisierbaren Energie entwickelt (Moe, 1994), die der vom Körper nutzbaren Energie entspricht (physiologischer Brennwert).
Die chemische, metabolisierbare Energie der Nahrungsstoffe wird in einem nächsten Schritt vom Stoffwechsel in die körpereigenen energiereichen Verbindungen wie Kreatinphosphat und Adenosintriphosphat (ATP) umgesetzt. Dies bildet wiederum den Ausgangspunkt für mechanische Arbeit sowie die Synthese von Strukturproteinen, Enzymen et cetera. In Ruhe wird die dem Körper zugeführte Energie zum größten Teil in Wärme umgewandelt. Dabei entspricht die Wärmeabgabe dem Energieumsatz innerhalb des Organismus (bspw. Herz- und Atemmuskulatur, Stofftransport; Silbernagl & Despopoulos, 2012, S. 240). Wenn über einen gewissen Zeitraum der Energieverbrauch > Energiezufuhr ist (sog. negative Energiebilanz), so muss der Körper Energie für überlebenswichtige Prozesse aus den körpereigenen Energiespeichern beziehen. Dabei wird die genutzte Energie durch die Ernährung selbst (Leckey et al., 2018), aber auch durch die Belastungsintensität beim Sporttreiben beeinflusst (Jiang et al., 2020). Grundsätzlich kommt die Energie jedoch von allen 3 Makronährstoffen, wie pointiert von Minichowski (2020) auf den Punkt gebracht:
„Die Wahrheit ist indes, dass die Energienöte unseres Körpers aus einer Vielzahl von Kanälen gespeist werden. Ganz so, wie sich unser Hausstrom aus unterschiedliche Bezugsquellen, etwa Wind-, Wasser-, und Biogas, zusammensetzt, so wird der akute Energiebedarf des Körpers in Form eines Energie-Mix gedeckt, nämlich dem Kohlenhydrat-, Protein- und Fettstoffwechsel.“
Und wie funktioniert die Gewichtsabnahme jetzt genau?
Carbohydrate-Insulin-Model (CIM)
Die Gesetze der Thermodynamik gelten selbstverständlich auch für den menschlichen Körper. Dies wird nicht zuletzt Ausdruck im derzeit vorherrschenden CICO Modell, das die Energieveränderungen im Körper (Gewichtszu- bzw. Gewichtsabnahme) – etwas sehr simplifizierend – über die Ratio zwischen Energiezufuhr sowie Energieverbrauch erklärt. Dass einfache Erklärungen oftmals nicht alle Facetten des dynamischen Systems des menschlichen Körpers erklären können, führte in den letzten Jahren zur Formulierung eines Alternativmodells (CIM), das bis in die aktuelle Zeit von einigen Wissenschaftlern propagiert wird (Ebbeling et al., 2018; Ludwig & Ebbeling, 2018; Ludwig & Friedman, 2014; Ludwig, Lakin, Wong, & Ebbeling, 2019).
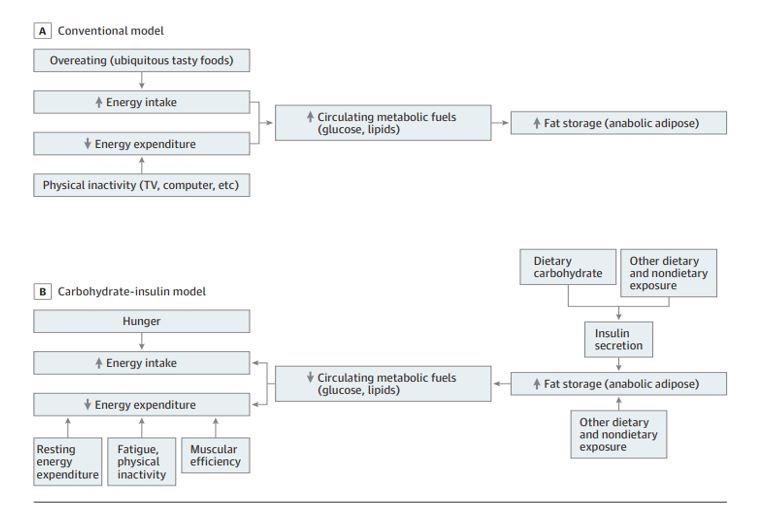
Abb. 2. Übersicht über das CIM (B) im Vergleich zum CICO Modell (A) (conventional model; Ludwig & Ebbeling, 2018, S. E2).
Das CIM legitimiert sich in erster Linie darüber, dass das vorherrschende CICO Modell die immer stärker werdende Übergewichtspandemie zum einen nicht gänzlich erklären, zum anderen aber auch scheinbar nicht bremsen kann – und das trotz des scheinbar einfachen Credos von eat less move more (Aragon et al., 2017, S. 10). Zur Legitimation des CIM werden Tierexperimente (Torbay, Bracco, Geliebter, Stewart, & Hashim, 1985) und genetische Modelle (Astley et al., 2018) angeführt. Auch suggerieren metanalytische Humandaten die angebliche Überlegenheit von low-carb-high-fat Diäten beim Gewichtsverlust (Mansoor, Vinknes, Veierød, & Retterstøl, 2016). Die Kernaussage des CIM beläuft sich schließlich darauf, dass Kohlenhydrate den Gewichtsverlust negativ beeinflussen sowie für die Übergewichtspandemie verantwortlich zu machen sind – und dementsprechend Kalorie ≠ Kalorie sei.
Die Aussagen des CIM basieren auf reduzierter alltäglicher Bewegung sowie auf einer Änderung in der Nahrungsqualität (bspw. hoch-prozessierte Lebensmittel). Die Folge, so das CIM, ist eine vermehrte Einlagerung der zugeführten Energie in Fettspeichern (Ludwig, 2002). Dies führt wiederum zu einer Negativschleife, da nun weniger Energie im Blut für physiologische Prozesse zur Verfügung steht (reduzierte Energy Availability) und dies mit einem Anstieg von Hunger sowie reduziertem Energieverbrauch einhergeht. In diesem Kontext verweist das CIM besonders auf die entscheidende Rolle der Fettzellen, die hierbei nicht nur Mediator der Hormone Ghrelin und Leptin sind, sondern im Wesentlichen über Insulin gesteuert werden. So sorgt Insulin bspw. für einen Anstieg der Glukoseaufnahme in das Zielgewebe, gleichermaßen aber auch für eine Inhibition der Fettsäurefreisetzung aus (Lipolyse) sowie einer Neuveresterung in das Fettgewebe (Lipogenese). In diesem Kontext verweist das CIM abermals auf die Rolle einfacher Kohlenhydrate, id est mit hohem glykämischem Index, die für einen vergleichsweise hohen und schnellen Insulinpeak sorgen. Zwar sei Protein teilweise genauso insulinogen (Ludwig & Ebbeling, 2018), protein-induzierte Sekretion von Insulin gehe aber auch immer mit einer Stimulierung von Glukagon, einem Insulinantagonisten einher, der diesen Effekt quasi abschwäche. Eine genauere Erklärung unterbleibt von den Autoren, leider.
Das Überangebot von einfachen Kohlenhydraten führt nach dem CIM zu einer postprandialen Hyperinsulinämie, d.h. zu einem Überangebot von Insulin nach Verzehr einer Mahlzeit, was wiederum in Einlagerung von Energie, statt Oxidation, resultiert. Ein ganz wichtiger Unterschied zum CICO Modell liegt darin, dass das CIM die stetige Zufuhr von hochgeschmacksvollem Essen als Konsequenz von einem steigendem Körperfettanteil sieht (anders als das CICO Modell, dass das Energieüberangebot für den steigenden Körperfettanteil verantwortlich macht). Daher, so das CIM, kann das Werkzeug der Energierestriktion nur als Symptombehandlung angesehen werden, die für die meisten Menschen aufgrund von steigendem Hunger in Folge der veränderten Nährstoffqualität, zum Scheitern prädestiniert sei. Im Kontext des Gewichtsverlustes sieht das CIM den zentralen Schlüsselfaktor also nicht unbedingt auf energetischer, sondern auf Ebene der Makronährstoffe. Dass diese „Alternativerklärung“ jedoch mit den Gesetzen der Thermodynamik kollidiert, scheint den Autoren nichts auszumachen.
CICO, Gewichtsverlust und das Prinzip der Energiebilanz
Das CICO Modell erklärt die Übergewichtspandemie anhand des Missverhältnisses von exzessiver Kalorienzufuhr und verrichteter Arbeit (u.a. Bewegung), was heutzutage hinreichend als Prinzip der Energiebilanz bekannt ist. So kommt es, aufgrund der positiven Energiebilanz, zu einem Überangebot an Substraten im Blut, was in einer Speicherung der überschüssigen Energie mündet (Ravussin et al., 1985). Demgegenüber resultiert eine negative Energiebilanz in einem Rückgriff auf gespeicherte Energie, um die entstehende Differenz zu relativieren. Damit wird das Verhältnis zwischen oben genannten Faktoren einzig und allein durch energetische Faktoren, unabhängig von Makronährstoff, -qualität und -timing, bestimmt (Buchholz & Schoeller, 2004). Die Energiebilanz lässt sich nach Loucks (2004) folgendermaßen mathematisch quantifizieren:

Da das CICO Modell durch einen breiten body of evidence gestützt wird, formulieren erste Fachgesellschaften (Schwartz et al., 2017) und position stands (Aragon et al., 2017) die Energiebilanz als den wesentlichen Eckpfeiler für Gewichtsabnahme in Abwesenheit von Krankheiten. Dies wird ferner von größer angelegten randomisiert kontrollierten Studien gestützt (Gardner et al., 2018) sowie durch qualitative (Systematic reviews) und quantitative (Metaanalysen) Publikationen belegt (Hall, 2017; Hall & Guo, 2017; Hooper et al., 2012; Howell & Kones, 2017). Unter Verweis auf die lipogene Funktion von Insulin wird oftmals geschlussfolgert, dass Insulin den Fettverlust negativ beeinflusst (Velasquez-Mieyer et al., 2003) – wie ebenfalls durch das CIM propagiert. Dies ist, zumindest auf kurze Sicht, auch wahr. Gleichermaßen stellt dies jedoch nur einen Schnappschuss eines hochdynamischen Prozesses dar, der nachfolgend kritischer Betrachtung erfährt.
Grundsätzlich sind immer Teile des Lipid- und Glukosemetabolismus‘ gleichzeitig aktiv. Der Wechsel zur Metabolisierung von Kohlenhydraten, sog. fuel shifts, ist dabei wesentlich von den verfügbaren Substraten und damit von Energiestatus und Ernährungsgewohnheiten abhängig (Spriet, 2014). In zeitlicher Perspektive entstehen fuel shifts dann, wenn postprandial Insulin ausgeschüttet wird.
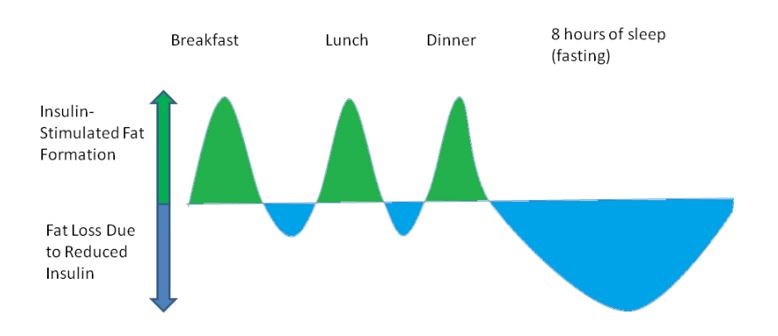
Abb. 3. Schematische Darstellung der Balance zwischen Lipogenese (gründe Fläche) und Lipolyse (blaue Fläche; Krieger, 2018).
Dies hat einen konstanten Turnover zwischen Lipolyse und Reesterifikation (Lipogenese) in den Fettspeichern zur Folge (Abb. 3). Das heißt, dass die Lipogenese (grün) postprandial die Lipolyse (blau) übersteigt. Beim Schlafen ist dies jedoch genau umgekehrt, sodass ein ausgeglichener Effekt nach einem bestimmten Zeitraum (sagen wir der Einfachheit halber 24 Stunden) zu beobachten ist – aber auch natürlich nur, wenn die Energiebilanz ausgeglichen ist. Denn das Verhältnis von Lipogenese und Lipolyse ist bekanntlich maßgebend von der Kalorienzufuhr abhängig: Übersteigt die Lipogenese die Lipolyse, so kann ein Gewichtszuwachs beobachtet werden (Kalorienüberschuss). Befindet sich der Mensch jedoch in einem Kaloriendefizit, also in einer negativen Energiebilanz, wird – trotz akuter Hemmung der Lipolyse postprandial – ein Gewichtsverlust erzielt. Somit ist nicht die Reduzierung der Kohlenhydrate (low-carb) der entscheidende Faktor für den Diäterfolg, sondern einzig und allein die Etablierung einer negativen Energiebilanz.
Die Hemmung lipolytischer Enzyme erfolgt postprandial durch Ausschüttung von Insulin (Watt et al., 2004). Gleichermaßen werden 3 freie Fettsäuren (FFS) und ein Glycerol-3-Phosphat Rest zu Triglyzeriden, der Speicherform im Fettgewebe, resynthetisiert (Campbell, Carlson, Hill, & Nurjhan, 1992). In Folge dessen kommt es zur Abnahme der Fettkonzentration im Blut sowie zu einer Unterdrückung der FFS Zufuhr in die Skelettmuskel (Stellingwerff & Cox, 2014). Dies verhindert schließlich, dass – neben den zugeführten Kalorien der Mahlzeit – ein Überangebot von Substraten im Blut entsteht. Eine solche Hemmung der lipolytischen Enzyme ist sowohl über cAMP-abhängige als auch -unabhängige Mechanismen erklärbar (Arner, 2005; Duncan, Ahmadian, Jaworski, Sarkadi-Nagy, & Sul, 2007). Die Schnittmenge aller Mechanismen liegt in der reduzierten Aktivierung der Hormon-sensitiven Lipase (HSL), einem Enzym, das wesentlich bei der Spaltung von Triglyzeriden beteiligt ist (Arner, 2005; Ragolia & Begum, 1998).
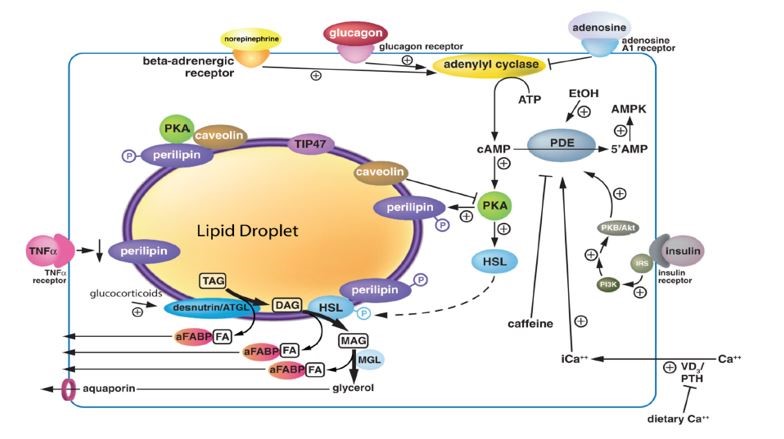
Abb. 4. Regulation der Lipolyse in Adipozyten (Duncan et al., 2007, S. 22).
In Abwesenheit von Nahrung (z.B. beim Fasten), beim Sporttreiben und generell unter hypokalorischen Bedingungen sinkt das Insulinlevel im Blut, während Adrenalin-, Glukagon- und Kortisolkonzentrationen ansteigen (Perea, Clemente, Martinell, Villanueva-Peñacarrillo, & Valverde, 1995). Glukagon sorgt ferner für einen Anstieg in der Adenylylcyclase-Aktivität (vgl. Abb. 4), was sich wiederum in einem Anstieg von intrazellulärem cAMP (als second messenger) in den Adipozyten, den Fettzellen, äußert (Perea et al., 1995). Für ein extensives Review sei auf Carmen & Víctor (2006), Duncan et al. (2007) bzw. Large, Peroni, Letexier, Ray und Beylot (2004) verwiesen.
Dies führt wiederum zu einem Anstieg der Lipolyse und damit zu einem Anstieg der Hydrolyserate von Triglyzeriden, um einem Substratmangel entgegenzuwirken. Folglich steigt die FFS Konzentration im Blut. Die Lipolyse wird jedoch keinesfalls nur durch die Aktionen der HSL gesteuert (Duncan et al., 2007); an dieser sind vielmehr auch andere Enzyme, wie bspw. Adipozyten Triaglycerol Lipase (Zimmermann et al., 2004), Desnutrin (Villena, Roy, Sarkadi-Nagy, Kim, & Sul, 2004) und Adiponutrin (Baulande, Lasnier, Lucas, & Pairault, 2001) beteiligt. Eine vermehrte Ausschüttung der Enzyme ist bspw. besonders nach Muskelkontraktionen zu beobachten (Jocken & Blaak, 2008), gefolgt von Triglyzeridspaltung sowie einer anschließenden Freisetzung von FFS und Glycerol ins Blut (Duncan et al., 2007). Innerhalb dieser Triglyzeridhydrolyse werden Triglyzeride zu Diacylglycerol und einer FFS und weiter zu Monoacylgylcerol sowie einer FFS gespalten. Schließlich erfolgt die Hydrolyse zur letzten FFS und dem Glycerol-Rest, dem Transport zum Zielgewebe sowie einer anschließenden Oxidation (Energiegewinnung) oder eben der erneuten Reesterifikation (konstanter Turnover). Unter hypokalorischen Bedingungen werden Adipozyten entleert, sodass diese in ihrer morphologischen Größe schrumpfen (Duncan et al., 2007). Rechnerisch bedarf es hierzu einer Einsparung von ca. 7000 kcal, um 1 Kilogramm Fett zu verlieren (Hall, 2008).
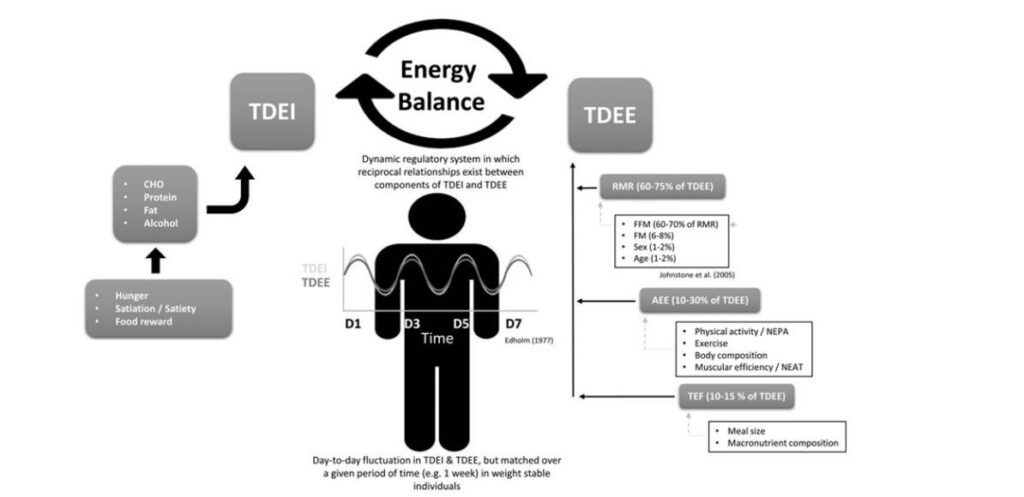
Abb. 5. Schematischer Überblick über Faktoren, die die tägliche Energiebilanz beeinflussen (Casanova, Beaulieu, Finlayson, & Hopkins, 2019, S. 3). Legende: TDEI = Energiezufuhr; CHO = Kohlenhydrate; TDEE = Energieverbrauch; RMR = Grundumsatz; FFM = fettfreie Masse; FM = Fettmasse; AEE = Aktivitätsenergieverbrauch; NEAT = bewusste und unbewusste Bewegung; TEF = nahrungsinduzierte Thermogenese.
Calorie „in“
Die Energiebilanz setzt sich aus der täglichen Energiezufuhr („in“ Seite) sowie des täglichen Energieverbrauchs („out“ Seite) zusammen. Dies findet sich überblicksartig in Abb. 5 illustriert. Grundsätzlich ist dabei die Energiebilanz recht einfach beschrieben: Der Körper verbraucht und verliert tagtäglich Energie, die dieser aus verschiedenen Energiequellen wiederherstellen muss (Taeger, 2018, 23f.; ebd., S. 28).
Unverkennbar wird die Energiezufuhr durch den täglich Konsum von Nahrung und Getränken (Alkohol und zuckerhaltig) beeinflusst. Überdies gibt es Einflussfaktoren (z.B. Hungergefühl), die auf das Essverhalten einwirken. Lange Zeit wurde in dieser Hinsicht davon ausgegangen, dass Veränderung der Fettmasse und periphere Veränderungen der Leptinkonzentrationen für die Veränderungen im Hungergefühl verantwortlich waren (Perry & Wang, 2012). So zeigte sich bspw. ein gesteigertes Hungergefühl sowie eine gesteigerte Energiezufuhr bei niedrigem Leptinspiegel (Sainsbury & Zhang, 2010). Inzwischen werden solche Veränderungen jedoch gleichermaßen durch gesteigerte Ghrelin (Cummings, Frayo, Marmonier, Aubert, & Chapelot, 2004) sowie sinkende Cholezystokinin (CCK), Peptide YY (PYY) und Glucagon-Like Peptide 1 (GLP-1) Konzentrationen (Sumithran et al., 2011) erklärt, die allesamt zu einem Anstieg von Hunger führen und eine Art „biologischen Druck“ aufbauen, der wiederum zu einer gesteigerten Energiezufuhr führt (Maclean, Blundell, Mennella, & Batterham, 2017). Das Essverhalten wird zumal wesentlich durch suffizienten Schlaf beeinflusst, wobei durch weniger Schlaf die Wahrscheinlichkeit steigt, mehr Kalorien zu sich zu nehmen (Chaput, 2010; Dashti, Scheer, Jacques, Lamon-Fava, & Ordovás, 2015).
Um die Faktoren, die auf die „in“ Seite einwirken, zu quantifizieren wird daher oftmals auf Self-Tracking zurückgegriffen. Überraschenderweise kommt es jedoch ab und an, und das trotz einer vermeintlich negativen Energiebilanz, zu keinem nennenswerten Gewichtsverlust. Und auch wenn die Gründe hierfür vielseitig sein mögen, so wird doch hauptsächlich ein „eingeschlafener“ oder „kaputter Stoffwechsel“ (ergo in Relation zur „out“ Seite) für den ausbleibenden Gewichtsverlust verantwortlich gemacht oder gar die Gesetze der Thermodynamik gänzlich in Frage gestellt (so bspw. im CIM). Während ein zu kleiner Zeitraum im Anfall von Ungeduld oder großer Alltagsstress durchaus als mögliche Gründe für fehlenden Gewichtsverlust verantwortlich sein können (bspw. durch eine verstärkte Wasserretention), so sind es tatsächlich vielmehr die kleinen und offensichtlichen Dinge auf der „in“ Seite, die eine Diät zu torpedieren scheinen: Hierbei sei bspw. auf Kalorie-Underreporting bis zu 47% und Overreporting von physischer Aktivität von bis zu 53% verwiesen (Lichtman et al., 1992). Hinzutreten, wie im Energiekapitel angedeutet, Rundungsfehler bei der Berechnung der Makronährstoffenergie, Differenzen im Ballaststoffanteil der Ernährung (Miles, Kelsay, & Wong, 1988) sowie Fehler bei der Nutzung verschiedener Essendatenbanken, die leider oftmals einen hohen Standardfehler aufweisen. Wird die „in“ Seite in Folge solcher Fehler nicht richtig quantifiziert, kann keinerlei Aussage bzgl. der Energiebilanz getroffen werden. Solche Unklarheiten sollten indes aber nicht als thermodynamischer Vorteil einer spezifischen Ernährungsform interpretiert werden.
Calorie „out“
Der tägliche Energieverbrauch, also die „out“ Seite des Modells, setzt sich durch willentlich und unwillentlich-beeinflussbare Faktoren zusammen. Dieser „Gesamtenergieverbrauch“ (TEE) besteht demnach, wie Abb. 6 zeigt, aus unterschiedlichen Teilsystemen:
- dem Grundumsatz, der zwischen 60-70% des Gesamtenergieverbrauchs ausmacht.
- der nahrungsinduzierten Thermogenese (TEF, thermic effect of food), die mit 8 bis 15% zum Gesamtenergieverbrauch beiträgt.
- der (un-)bewussten Bewegung (NEAT, non-exercise activity thermogenesis), die ungefähr 15-30% ausmacht.
- dem Training (EAT, exercise activity thermogenesis), das, je nach Trainingsart und -umfang, zu einem variablen Anteil zum TEE gerechnet werden kann.
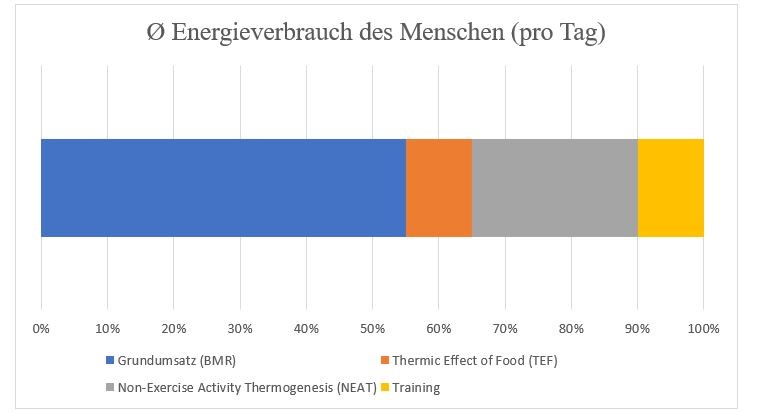
Abb. 6. Der tägliche Energieverbrauch des Menschen in Anlehnung an Ravussin und Bogardus (1989) und Westerterp (2013).
Die genannten Zahlen sind konsequenterweise nur als Durchschnittwerte zu interpretieren, welche sich meist auf sesshafte Populationen beziehen. Steigt das Trainingspensum stark an, wie es bei Sportlern der Fall ist, so sinken zwangsläufig die Kontributionen von Grundumsatz, TEF und NEAT anteilsmäßig.
Der Grundumsatz ist dabei die Energiemenge, die zum reinen Erhalt des Körpers in Ruhe benötigt wird (Taeger, 2018, S. 28). Grundsätzlich kann der individuelle Grundumsatz dadurch ermittelt werden, dass die Atemgase einer Person über einen gewissen Zeitraum in Ruhe gemessen werden (indirekte Kalorimetrie). Die Ergebnisse werden dann auf den Tag hochgerechnet und ergeben den täglichen Grundumsatz. Abseits dieser Methode kann der Grundumsatz auch einfacher, aber ungenauer, über mathematische Formeln, sog. Regressionsgleichungen, bestimmt werden. Während nachfolgende Autoren einen Überblick über den Anwendungsbereich solcher Formeln liefern (Engeroff, Berk, Stücher, & Banzer, 2018), wird in wissenschaftlichen Arbeiten oftmals die Cunningham Formel herangezogen (Cunningham, 1980; Haaf & Weijs, 2014). Grundsätzlich werden, je nach Genauigkeit der Formel, soziodemographische und anthropometrische Faktoren berücksichtigt (Alter, Geschlecht) sowie endogene (z.B. Skelettmuskelmasse, Fettmasse) und exogene (z.B. Ernährung) Einflussfaktoren miteinbezogen (Johnstone, Murison, Duncan, Rance, & Speakman, 2005).
Der Grundumsatz setzt sich aus 60-70% des TEE zusammen und wird im Wesentlichen durch metabolisch-aktives Gewebe beeinflusst, d.h. durch Organe bzw. durch die Skelettmuskelmasse. Da Frauen im Schnitt weniger Muskelmasse als Männer haben, aber auch beim gleichen Geschlecht große Unterschiede bzgl. der Verteilung dieser herrschen, weist der Grundumsatz eine interindividuelle Variabilität auf (Stubbs et al., 2018). Während Phasen von Energierestriktion sinkt der Grundumsatz, wobei auch hier die Höhe interindividuell variabel ist (Müller et al., 2015; Müller & Bosy-Westphal, 2019; Müller, Enderle, & Bosy-Westphal, 2016). Dies ist, zumindest meistens, durch den Verlust von Muskelmasse bzw. metabolisch-aktivem Gewebe zu erklären. Je nach Planung der Diätstrategie sowie der untersuchten Population liegt die Varianz der Muskelmassenveränderung irgendwo zwischen Muskelmassenzuwächsen (Trainingsanfänger, Frauen) und hohen Muskelmassenverlusten (fortgeschrittener Kraftsportler mit schlecht geplanter Diät). Ein Abfall des Grundumsatzes erklärt somit auch die anfänglich schnellere Gewichtsverlustrate, die, mit fortschreitender Diät, immer weiter abzuflachen scheint (vgl. Abb. 7; Weck, Bornstein, Barthel, & Blüher, 2012). Eine Reduktion des Grundumsatzes (5-10%) kann dabei schon nach 2 Tagen Diät gemessen werden und wird u.a. durch ein Anstieg der Gluconeogenese-Aktivität, der Neubildung von Glukose in der Leber, erklärt (Siw Eriksson, Olsson, & Björkman, 1988). Wertvolle Maßnahmen gegen den Abfall des Grundumsatzes sind eine proteinlastige Makronährstoffverteilung sowie die Durchführung von RT (Bryner et al., 1999).
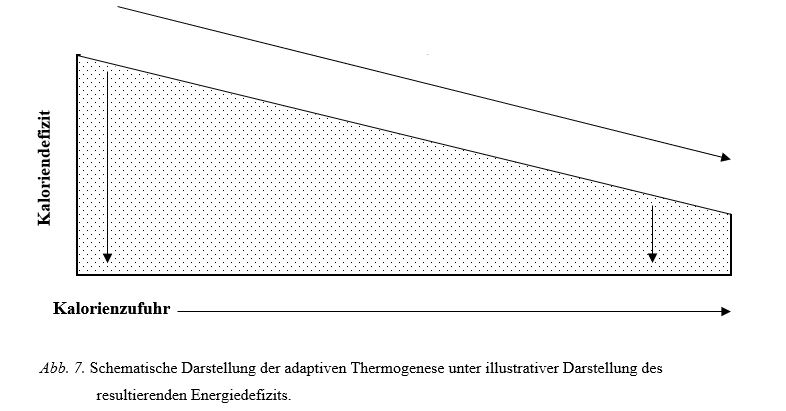
Oftmals fällt der Energieverbrauch des Körpers im Laufe hypokalorischer Bedingung jedoch weiter ab als durch eine Veränderung der Körperkomposition erklärt werden kann. Dieser Prozess wird adaptive Thermogenese genannt (Camps, Verhoef, & Westerterp, 2013) und ist, im Kontext eines Energiemangels, leicht zu erklären (Trexler, Smith-Ryan, & Norton, 2014). Der Körper spart sich die Energie für wichtige physiologische Überlebensprozesse und reduziert gleichermaßen „unwichtige“ und energieaufwändige Prozesse, wie bspw. die Neubildung von (Muskel-)Proteinen (Browne & Proud, 2002; Witard, Garthe, & Phillips, 2019). Ein solcher Abfall der Proteinsynthese ist somit auch als primärer Grund zu nennen, warum muskuläre Atrophie in Zeiten von Energierestriktion auftritt. Auch wenn der Anpassungseffekt der adaptiven Thermogenese bisher gleichermaßen kritisch in Frage gestellt wird (Flatt, 2007), scheinen ein Verlust von Organzellmasse (Gallagher et al., 2017), reduzierte Schilddrüsenaktivität (Tremblay, Royer, Chaput, & Doucet, 2013) sowie gesteigerte muskuläre Effizienz (Rosenbaum et al., 2003) allesamt zu einem Abfall auf der „out” Seite beizutragen. Das bedeutet wiederum, der Körper wird innerhalb einer Diät effizienter bei der Einteilung der eigenen Energieverfügbarkeit. Und auch wenn die einzelnen Teilsysteme des TEE nicht oder nur leicht auf die Energierestriktion reagieren, so kann die Summe aller Teilsysteme doch erheblichen Einfluss auf den Diätfortschritt entfalten.
Ein wesentliches Teilsystem in diesem Kontext ist der TEF, der zum täglichen Gesamtenergieverbrauch des Körpers beiträgt. Dieser wird als diejenige Energie quantifiziert, die postprandial die metabolische Rate ansteigen lässt und umfasst die verbrauchte Energie für die Verarbeitung der zugeführten (Nahrungs-) Energie (Verdauung usw.). Der TEF ist maßgeblich von der Menge und Zusammensetzung der zugeführten Nahrung abhängig und beträgt ca. 10% der zugeführten Energie (Hall et al., 2012). Die oben aufgeführten Schwankungen zwischen 8-15% des TEE werden auf die Betrachtung unterschiedlicher Makromoleküle zurückgeführt. In Übereinstimmung mit Loeffelholz und Birkenfeld (2000) berichten Halton und Hu (2004) einen thermic effect of protein von 25-30% und einen thermic effect of carbohydrate von 5-15%. Die Studienlage zum thermic effect of fat ist bisher nicht eindeutig, beziffert sich aber, je nach untersuchten Fetten, auf 0-5%. Wichtig zu erwähnen bleibt, dass der TEFder einzelnen Makronährstoffe auf Basis unterschiedlicher molekularer Strukturen variieren kann: So zeigte sich bspw. ein deutlich höherer TEF nach Konsum von mittelkettigen im Vergleich zu langkettigen Fettsäuren (Seaton, Welle, Warenko, & Campbell, 1986) oder ein höherer TEF im Vergleich von Whey und Casein (Acheson et al., 2011). Grundsätzlich scheinen unverarbeitete Lebensmittel auch einen höheren TEF aufzuweisen (Barr & Wright, 2017). In Bezug zur Diät sollte klar sein, dass der TEF gleichermaßen abfällt. Dies ist einfach durch die reduzierte Substratversorgung zu erklären. Auch wenn die Reduktion des TEF durch eine proteinbetonte Ernährung weitgehend inhibiert werden kann (Drummen et al., 2019), scheint ein 10%iger Rückgang des TEF trotzdem wahrscheinlich (Bessard, Schutz, & Jéquier, 1983).
Als NEAT werden zumal alle Aktivitäten des täglichen Lebens zusammengefasst, die keinem klassischen Workout zugeordnet werden. Hierbei zählen u.a. berufliche Tätigkeiten, Freizeitaktivitäten, einfaches Herumlaufen, aber auch unbewusste Aktivitäten wie das „Zappeln“ mit den Beinen. Je nach beruflicher Tätigkeit können sich hier schon große Unterschiede bemerkbar machen. Wird bspw. eine überwiegend sitzende Bürotätigkeit mit einer Tätigkeit verglichen, bei der ständig Bewegung vorhanden ist (z.B. als Lehrkraft), kann sich hier ein täglicher Kalorienunterschied von bis zu 2000 kcal bei Personen mit ähnlichen anthropometrischen Eigenschaften bemerkbar machen (Levine, 2007). In hochaktiven Individuen bestimmt der NEAT bis zu über 50% des täglichen Gesamtenergieverbrauchs (Levine, 2004). Während der NEAT somit als interindividuell hochvariabel beschrieben werden muss, fluktuiert dieser auch intraindividuell. So kann dieser im Rahmen eines Kaloriendefizits gleichermaßen, bewusst oder unterbewusst, durch weniger Bewegungslust abfallen (Racette, Schoeller, Kushner, Neil, & Herling-Iaffaldano, 1995; Weigle, 1988). Ein kürzlich erschienenes Systematic review kommt zum Schluss, dass in Zeiten der Energierestriktion eher unwillentliche statt willentliche Bewegungen abfallen (Silva et al., 2018). Zum TEE wird schließlich noch die Energie hinzugefügt, die bei den eigentlichen Trainingseinheiten anfallen.
Eine zu starke Vereinfachung des CICO Modells hat schließlich zum Credo eat less move more geführt (Aragon et al., 2017, S. 10), an dem technisch auf den ersten Blick nichts falsch zu sein scheint. Wie gerade aufgezeigt, ist eine derartige Simplifizierung jedoch nicht haltbar, da der Körper metabolischen Anpassungsprozessen während Zeiten von Energierestriktion unterliegt (Trexler et al., 2014), die weitreichende Folgen auf die Höhe des Energieverbrauchs auf der „out“ Seite haben. Die Herausforderung für eine gelingende Diät liegt demnach darin, sich nicht einfach mehr zu bewegen und weniger zu essen, sondern alle wichtigen Faktoren so zu berücksichtigen, sodass die angestrebte Körperkomposition erreicht und eine Reduzierung des Grundumsatzes vermieden wird. Unter Verweis auf genetische Prädispositionen ist aktuell unklar, ob es tatsächlich einen Phänotyp gibt, der als Gewichtsverlust-resistent bezeichnet werden kann. Wenn ja, dann würde dieser wahrscheinlich durch einen größer als vorhersagbaren Abfall der „out“ Seite charakterisiert sein (Casanova et al., 2019)
Negative Energiebilanz, aber wie hoch? – Praktische Implikationen
Die Energiebilanz entscheidet nicht nur dichotom über die Frage Gewichtsverlust/Gewichtzunahme, sondern gibt auch Aufschluss über die Höhe der Anpassungen. Und auch wenn hohe Stresslevel und endokrine Veränderungen (z.B. durch die Monatsblutung) für eine vermehrte Wasserretention sorgen oder Muskelaufbau während der Diät keinen Gewichtsdrop auf der Waage erkennen lässt, so diktieren die Gesetze der Thermodynamik doch eine Transformation von Energie. Das heißt, auch wenn die Waage, die demnach kein reliabler Indikator für den Verlust von Fettmasse ist, keinen Gewichtsverlust anzeigt, so verliert – natürlich nur unter der Voraussetzung eine konstant-negativen Energiebilanz – der Körper Fettmasse.
Aus der Formel von Loucks (2004) lässt sich schließlich ableiten, dass mit steigendem Defizit über einen festgelegten Zeitraum auch die Höhe des Gewichtsverlusts über einen bestimmten Zeitraum steigt. Je länger dieser Zustand aufrechterhalten wird (Länge der Diät) desto größer wird auch der Gewichtsverlust. Um mögliche Nährstoffdefizienzen, Negativanpassungen auf der „out“ Seite sowie den Verlust von Muskelmasse zu minimieren, scheint daher eine umsichtige Planung aller relevanten Faktoren (Alter, Geschlecht, Sportart, Trainingspensum, Trainingserfahrung, Zielsetzung, Diätlänge, Anzahl der Diättage pro Woche, monetäre Faktoren, etc.) unumgänglich.
Dass sich der Gewichtsverlust in einer Diät rein auf den Verlust von Fettmasse (FM) beschränkt, ist eine Illusion. Vielmehr verliert der Körper u.a. auch Muskel-, Organ- und Knochensubstanz, die sog. fettfreie Masse (FFM; Nicklas et al., 2015). Durch die Höhe des Energiedefizits wird die Komposition der verlorenen Masse stark beeinflusst (Ashtary-Larky et al., 2017; Gallagher et al., 2000): So steigt die Wahrscheinlichkeit für FFM-Verlust sowohl mit der Höhe des Kaloriendefizits (Garthe, Raastad, Refsnes, Koivisto, & Sundgot-Borgen, 2011) als auch mit verringerter Energy Availability (Fagerberg, 2018). Während letztere die Menge an Energie ist, die, nach Abzug von sportlicher Aktivität, wirklich noch für physiologische Prozesse herangezogen werden kann (zur Quantifikation dieser, vgl. Heikura et al., 2018), findet sich eine komplette Auflistung über FFM-beeinflussende Faktoren bei Heymsfield et al. (2011). Hierzu zählen u.a. die tägliche Proteinmenge (vgl. Artikel II dieser Reihe; Pasiakos et al., 2013), der Einsatz von Krafttraining und die richtige Applizierung der Belastungsnormative (vgl. Artikel III dieser Reihe; Calbet et al., 2017), Trainingserfahrung (Avila, Gutierres, Sheehy, Lofgren, & Delmonico, 2010; Kistler, Fitschen, Ranadive, Fernhall, & Wilund, 2014) sowie Ausgangskörperfettanteil (KFA; Forbes, 2000).
Um möglichst wenig Muskelmasse zu verlieren, muss a) die tagtägliche Energie vornehmlich aus Fett- und Glykogenspeichern bzw. aus Glukose bezogen werden und b) etwaige Beiträge aus dem Proteinstoffwechsel (d.h. bspw. durch Abbau von Muskulatur) täglich resynthetisiert werden (hier benötigen wir ergo ein Equilibrium zwischen der Proteinsynthese, sowie dem Abbau von Proteinen, dem sog. Proteinbreakdown. Leider gibt uns eine klassische Waage keine Auskunft über die Zusammensetzung des verlorenen Gewichts. Dafür bräuchte man, sofern gewünscht, ein Gerät, dass den Gewichtsverlust quantifizieren kann. Eine Möglichkeit wäre hierbei der Einsatz einer bioelektrischen Impedanzanalyse (BIA), die, im billigsten Fall, auch oftmals in einer Personenwaage eingebaut ist. Da dieser Methodenaspekt jedoch nicht den Kernbereich des Artikels trifft, hier nur einige wenige Worte: Das Messverfahren der BIA darf nur unter hochstandardisierten Bedingungen interpretiert werden, da das Verfahren einem hohen Standardfehler unterliegen kann. Wenn dies eingehalten wird, könnte die BIA u.U. (das ist wiederum Gerätabhängig) reliable Werte liefern. Da beim Gewichtsverlust aber unterschiedliche Verluste von festen Stoffen (bspw. myofibrilläre Proteine) bzw. Wasser (z.B. Sarkoplasma) auftreten, sind auch BIA Werte weder eindeutig noch genau interpretierbar – liefern aber zumindest einen Trend.
Aber auch wenn der (mögliche) Verlust von Muskelmasse nicht valide quantifiziert werden kann, so stellt sich dennoch die Frage nach der bestmöglichen Präservation von FFM unter hypokalorischen Bedingungen. Hier bleibt zunächst festzuhalten, dass es das „perfekte Defizit“ nicht gibt. Vielmehr hängt die Wahl bezüglich der Höhe des Defizits von verschiedenen bereits genannten Faktoren, wie bspw. der eigenen Zielsetzung und der Diätlänge, aber auch vom KFA, den Trainingsmöglichkeiten sowie der finanziellen bzw. gesundheitlichen Situation ab. Grundsätzlich wurden bereits Defizite bis zu 3.2 kcal/kg Körpergewicht bei stark adipösen Individuen untersucht (Calbet, Ponce-González, Pérez-Suárez, La Calle Herrero, & Holmberg, 2015). Solche very-low-calorie Diäten (VLCD) sind ein beliebtes Werkzeug, um schnellstmöglich an Körpergewicht zu verlieren. Hier wird der Gedanke zu Grunde gelegt, respektive die Abwägung getroffen, dass eine Reduktion von Körpergewicht im gesundheitlichen Kontext sinnvoller erscheint als ein vollständiger Erhalt von Muskelmasse. Wird also die Abfederung der gesundheitlichen Nachteile eines stark erhöhten KFA als Primärziel formuliert, so kann ggf. auf solche VLCD zurückgegriffen werden. Dies darf jedoch nicht als Einladung für eine Crash-Diät interpretiert werden: Denn auch wenn stark übergewichtige Individuen vergleichsweise mehr Muskelmasse präservieren als leane Sportler, bedarf es immer, selbst bei hohem KFA, einer zielgerichteten und systematisch geplanten Diät (high-protein (HP), hohe mechanische Spannung sowie einer flexiblen und adhärenten Ausgestaltung), um a) Negativanpassungen auf der „out“ Seite abzufedern sowie b) die Retention von Muskelmasse und Grundumsatz zu ermöglichen.
Konsequenterweise ist ein hohes Defizit bei Kraftsportlern kaum zu empfehlen, selbst im Kontext eines sog. Minicuts. So wurde in einer brandaktuellen Untersuchung gezeigt, dass, nach nur 3 Tagen Energiedefizit (15kcal/kg FFM) bereits eine reduzierte endokrine Reaktion (IGF-1 ↓) auf die anabolen Reize von RT zu vernehmen war (Murphy & Koehler, 2020). Ein solcher Abfall wird anabolic resistance genannt und wird, wie oben beschrieben, durch eine reduzierte Elevation der Proteinsynthese erklärt, welche sich, so manche Autoren (Margolis et al., 2016), auf die Translation von physiologisch-wichtigen Proteinen konzentriert. Ein etwaiger Abfall der Proteinsynthese hat einen Anstieg der Ganzkörperproteolyse (Abbau von Proteinen), eine vermehrte Aminosäurenoxidation sowie eine erhöhte Stickstoffausscheidung zur Folge (Pasiakos et al., 2010). Diese anabolic resistance nimmt, so unser educated guess, mit fortschreitender Trainingserfahrung zu. In einer solchen Population sollte, sofern der bestmögliche Erhalt von Muskelmasse als Ziel formuliert wird, auf ein moderates Energiedefizit zurückgegriffen werden.
Dies bestätigten auch Areta et al. (2014): In ihrer Studie an fortgeschritten Kraftsportlern waren 15kcal/kgFFM nicht ausreichend (unter Zunahme von HP×RT), um eine vollständig stimulierte Proteinsynthese zu gewährleisten. Der Begriff „vollständig stimuliert“ bezieht sich dabei auf die postprandiale Elevation der Proteinsynthese unter eukalorischen Bedingungen. In selbiger Studie wurde zumal ein Kaloriendefizit 30kcal/kgFFM zu Grunde gelegt, welches ausreichend war, um die Proteinsynthese auf eukalorisches Niveau zu heben (Areta et al., 2014; Smiles et al., 2015). Werden diese Zahlen in Beispiele umgesetzt (80kg Mann, 60kg FFM), so zeigt sich eine Beispielkalorienzufuhr in der Calbet-Studie von 256kcal pro Tag sowie der Areta-Studie von 900kcal pro Tag (15kcal/kg FFM) bzw. 1800kcal pro Tag (30kcal/kg FFM). Um gesundheitliche Einschränkungen zu vermeiden (Mountjoy et al., 2014), wurde daher ein unterer Schwellenwert für Kraftsportlern bei ≥ 25 kcal/kg FFM festgelegt (Fagerberg, 2018). Dieser bezieht sich jedoch hauptsächlich auf gesundheitliche Faktoren (Hormone, Psyche, Muskelmasse und kardiovaskuläres System) und nicht, wie dieser Artikel forciert, auf den bestmöglichen Erhalt von Muskelmasse. So sehen wir, in Anlehnung an Areta et al. (2014), aber auch aus bisher noch unveröffentlichten Daten (Roth, Rettenmaier & Behringer, 2020), einen unteren Schwellenwert bei mind. 30kcal/kg FFM.
An dieser Stelle soll ebenfalls darauf hingewiesen werden, dass ein zu hohes Defizit zu schnelleren Anpassungen des Körpers („out“ Seite) und damit zur Reduktion des gewünschten schnelleren Abnehmens (Donnelly et al., 2009; Donnelly, Jakicic, & Gunderson, 1991) führt. Auch wenn dies bei bestimmten Populationen gerechtfertigt scheint (insbesondere im Kontext von starkem Übergewicht), so erhöhen hohe Kaloriendefizite gleichermaßen die Wahrscheinlichkeit zu Einbußen hinsichtlich Muskelmasse (Garthe et al., 2011; Karila et al., 2008; Kistler et al., 2014; Robinson, Lambeth-Mansell, Gillibrand, Smith-Ryan, & Bannock, 2015) und Performance im Kontext aktiver Individuen (Fogelholm, 1994; Jlid, Maffulli, Elloumi, Moalla, & Paillard, 2013; Mountjoy et al., 2018; Wilson et al., 2014). Dies ist insbesondere damit zu begründen, dass ein hohes Defizit Erholung sowie Trainingsleistung negativ beeinflussen kann, speziell wenn die Gesamtkalorien schon niedrig sind (Nattiv et al., 2007). Auch wenn Frauen im Schnitt mehr Muskelmasse halten als Männer, gelten auch hier die aufgeführten Grundgedanken. Während untrainierte Frauen bei einer gut geplanten Diät höchstwahrscheinlich die gesamte Muskelmasse halten (Avila et al., 2010), ist dies, unter optimalen Bedingungen, wahrscheinlich selbst bei Frauen während einer Bodybuilding-Wettkampfvorbereitung möglich (Petrizzo, DiMenna, Martins, Wygand, & Otto, 2017; Rohrig, Pettitt, Pettitt, & Kanzenbach, 2017; Tinsley et al., 2018). Ein solcher Unterschied zwischen Mann und Frau ist bspw. durch den Phänotyp, hormonelle Interaktionen oder durch die Mitochondrienaktivität zu erklären (Gurvich, Hoy, Thomas, & Kulkarni, 2018; Stapley, 2001; Williams, Walz, Lane, Pebole, & Hackney, 2015). Ein Überblick findet sich bei Rosa-Caldwell und Greene (2019).
Conclusio & Ausblick
Während besonders Interventionen auf energetischer Ebene (Energierestriktion) als wichtige Kontribution für gesundes Altern identifiziert wurden (National Academies Press (US), 2017), nimmt die Ernährung oftmals einen wichtigen Stellenwert im Leben von sportlichen Individuen ein. Diese ergänzt den Trainingsalltag, wirkt u.a. auf morphologische Adaptationen ein und dient als Werkzeug zur Erreichung fitnessspezifischer Ziele. Insbesondere ist dabei die Energiebilanz herauszustellen, die, im Rahmen des hier vorgestellten 4 Säulen Modells, zu einer erfolgreichen und gesunden Diät führt.
Der Körper ist dabei als (nicht-perfektes) System zu verstehen, das Energie konstant transformiert – nämlich von zugeführter Nahrung zur Produktion von Wärme. Da in diesem Kontext weder Energie erschaffen noch vernichtet wird, ist auch der Körper ein Organismus, der sich den formulierten Gegebenheiten der Thermodynamik beugt (1. Satz der Thermodynamik). Auf Basis dieser Erkenntnisse erklärt das CICO Modell die Gewichtszu- sowie Gewichtsabnahme durch die Energiebilanz. Dieses zwei-Faktoren Modell ist jedoch so simplifiziert, dass es weder gänzlich diätbedingten Anpassungsreaktionen Rechnung trägt noch die Übergewichtspandemie hinreichend erklären kann. Das wiederum begünstigte den wissenschaftlichen Diskurs um das CIM, welches keine überzeugenden Daten liefert und auch sonst die Grundlagen der Thermodynamik außer Acht lässt. So wurde im Artikel bereits kritisch dargelegt, dass Insulin seinem Ruf als „Anti-Gewichtsverlustshormon“ gar nicht unbedingt gerecht wird.
Doch auch wenn daher sinnvollerweise am CICO Modell festgehalten wird (Schwartz et al., 2017) und weiterhin Kalorie = Kalorie auf thermodynamischer Ebene bleibt, kann das CICO Modell nur bedingt als mathematisches Modell zur Vorhersage von Gewichtsverlust genutzt werden. Dies wird auf der „in“ Seite mit dem Konzept der metabolisierbaren Energie, den in Kauf genommen Mittelwerten bei den Atwater-Faktoren (Buchholz & Schoeller, 2004) sowie durch ungenaues Kalorienzählen begründet und auf der „out“ Seite durch diät-induzierte Anpassungen (adaptive Thermogenese) des TEE, etwa im Rahmen eines reduzierten Grundumsatzes, TEF oder NEAT, erklärt. Schließlich sind Messungenauigkeiten und metabolische Anpassungsprozesse der Grund dafür, dass entweder kein Gewichtsverlust zu Stande kommt, dieser von Wasserretentionen überschattet wird oder dieser im Laufe der Diät abzuflachen droht. Eines bleibt in diesem Kontext jedoch klar – ein konstantes Energiedefizit, irrelevant wie groß oder klein dieses auch sein mag – führt zu Gewichtsverlust. Und das auch, wenn die Waage, die nebenbei absolut kein verlässlicher Indikator für Fettverlust ist, diesen nicht sofort wiederspiegelt. Um langfristig eine Diät optimal planen zu können, stellt Corpus Novum daher ein kostenloses Tool zur privaten Nutzung zur Verfügung: Dieses ist auf 10 Wochen ausgelegt, schafft einen funktionalen Überblick über Kalorien, Proteine und Bewegung und gibt eine graphische Darstellung des Diätverlaufs inklusive Trendlinie, Zeit bis zur Zielerreichung und ein rechnerischen Kaloriendefizit wieder. Klicke hier zum kostenlosen Download.
Während das CICO Modell die Gewichtszu- und Gewichtsabnahme auf rein technisch-energetischer Ebene dementsprechend hinreichend zu erklären scheint, so stellt dieses keinerlei Informationen über die Komposition des abgenommenen Gewichts an. Denn auch wenn die Höhe des Kaloriendefizits maßgeblich auf die Komposition des Gewichtsverlustes einwirkt, bestimmen Faktoren auf Ebene der Makronährstoffe (u.a. auch Qualität und Timing), physische Aktivität und Schlaf die Präservation von FFM und Grundumsatz. Dies ist über positive Effekte auf den Proteinstoffwechsel zu erklären. Konkludierend heißt das dementsprechend, dass eat less move more eine nur halb-richtige Antwort für Gewichtsverlust ist: ein gesunder, nachhaltiger und demnach auch erfolgreicher Gewichtsverlust kann nur zustande kommen, wenn die obenstehenden Variablen zielführend und systematisch in Position gebracht werden.
Auch wenn es enttäuschend klingen mag, das universal-perfekte Energiedefizit gibt es nicht. Während mickrige Kaloriendefizite die Diät nur ungemein in die Länge ziehen, so tragen zu hohe Defizite zu einem verringerten anabolen Reiz sowie zu einer höheren anabolic resistance bei. Das zu wählende Defizit bestimmt sich ergo in Abhängig der zu Grunde gelegten Population. Grundsätzlich sollte die Höhe des Defizits weiterhin von Zielsetzung, Ausgangskörperfettanteil und Trainingserfahrung abhängig gemacht werden. Hierbei könnten leane Individuen im Sinne des Erhalts von FFM auf ein Defizit zwischen 500-1000 Kalorien zurückgreifen (Fogelholm, 1994; Rankin, 2002), während übergewichtige Individuen wohl auch höhere Defizite tolerieren (Seimon et al., 2019). Grundsätzlich gilt jedoch: mit höheren Defiziten steigt die „Gefahr“ des Verlusts von FFM (Garthe et al., 2011).
Zum Abschluss möchten wir dennoch einige warnende Hinweise liefern: Auch wenn die negative Energiebilanz als Voraussetzung für Gewichtsverlust sowie Krafttraining und eine proteinreiche Ernährung als Voraussetzung für Muskelmassenerhalt von Nöten ist, so ist das Treffen von bestimmten Makronährstoffzielen nur eine Seite der Medaille. Die andere Seite, die sich hauptsächlich durch das Stichwort Gesundheit charakterisieren lässt, ist maßgebend von der Zusammensetzung der zugeführten Nahrung abhängig. So sei beispielhaft auf Ballaststoffe und Mikronährstoffe verwiesen (Stichwort: Obst und Gemüse; Kirchhoff, 2019), die u.a. zu einem gesunden Mikrobiom beitragen, aber auch als Ko-Faktoren für die Biochemie des menschlichen Körpers dienen. Ohne ausreichende Obst- und Gemüsezufuhr wäre die Diät schnell torpediert und Mangelerscheinungen omnipräsent.
Aufbauend auf den bisher erbrachten Empfehlungen zur Energiebilanz bleibt schließlich die Frage offen, wie sich die Nährstoffe (v.a. die Makronährstoffe) in der Diät zusammensetzen sollten, um bestmöglich das Ziel des Gewichtsverlusts, aber auch der bestmöglichen Retention von Muskelmasse, zu erreichen. Genau diese Fragestellung verfolgen wir im zweiten Artikel der Reihe, der zweiten Säule einer gelungenen Diät. Hier werden wir insbesondere darlegen, wie die Proteinzufuhr zu einer verstärkten Synthese von Proteinen sowie zu einer Inhibition der Proteindegradation führt. Während in der dritten Säule additional die Effekte von Krafttraining eingehend untersucht und dargelegt werden, erfolgt in der letzten Säule sodann die Fokussierung auf einen weiteren, nicht zu unterschätzenden Aspekt: den psychologischen Einflussfaktoren. Da der menschliche Körper einem ständigen Aus- und Einbau von Nährstoffen unterworfen ist, fällt insbesondere dem konsistenten Überdauern, dem zeitlichen Aspekt der Diät, ein gewichtiger Stellenwert zu. Wir müssen uns demnach sowohl von dem Gedanken verabschieden, dass uns ein Tag Diät zu unserem Wunschgewicht bringen wird als auch, dass ein Tag in einer positiven Energiebilanz „fett macht“. Durch langfristige Planung, Beständigkeit und das Verfolgen des vorher festgelegten Ziels können eben diese Ziele erreicht und eine Diät erfolgreich abgeschlossen werden.
Referenzen
References
Acheson, K. J., Blondel-Lubrano, A., Oguey-Araymon, S., Beaumont, M., Emady-Azar, S., Ammon-Zufferey, C., . . . Bovetto, L. (2011). Protein choices targeting thermogenesis and metabolism. The American journal of clinical nutrition, 93(3), 525–534. https://doi.org/10.3945/ajcn.110.005850
Aragon, A. A., Schoenfeld, B. J., Wildman, R., Kleiner, S., VanDusseldorp, T., Taylor, L., . . . Antonio, J. (2017). International society of sports nutrition position stand: Diets and body composition. Journal of the International Society of Sports Nutrition, 14, 16. https://doi.org/10.1186/s12970-017-0174-y
Areta, J. L., Burke, L. M., Camera, D. M., West, D. W. D., Crawshay, S., Moore, D. R., . . . Coffey, V. G. (2014). Reduced resting skeletal muscle protein synthesis is rescued by resistance exercise and protein ingestion following short-term energy deficit. American Journal of Physiology. Endocrinology and Metabolism, 306(8), E989-97. https://doi.org/10.1152/ajpendo.00590.2013
Arner, P. (2005). Human fat cell lipolysis: Biochemistry, regulation and clinical role. Best Practice & Research. Clinical Endocrinology & Metabolism, 19(4), 471–482. https://doi.org/10.1016/j.beem.2005.07.004
Ashtary-Larky, D., Ghanavati, M., Lamuchi-Deli, N., Payami, S. A., Alavi-Rad, S., Boustaninejad, M., . . . Alipour, M. (2017). Rapid Weight Loss vs. Slow Weight Loss: Which is More Effective on Body Composition and Metabolic Risk Factors? International Journal of Endocrinology and Metabolism, 15(3), e13249. https://doi.org/10.5812/ijem.13249
Astley, C. M., Todd, J. N., Salem, R. M., Vedantam, S., Ebbeling, C. B., Huang, P. L., . . . Florez, J. C. (2018). Genetic Evidence That Carbohydrate-Stimulated Insulin Secretion Leads to Obesity. Clinical Chemistry, 64(1), 192–200. https://doi.org/10.1373/clinchem.2017.280727
Avila, J. J., Gutierres, J. A., Sheehy, M. E., Lofgren, I. E., & Delmonico, M. J. (2010). Effect of moderate intensity resistance training during weight loss on body composition and physical performance in overweight older adults. European Journal of Applied Physiology, 109(3), 517–525. https://doi.org/10.1007/s00421-010-1387-9
Barr, S., & Wright, J. (2017). Postprandial energy expenditure in whole-food and processed-food meals: Implications for daily energy expenditure. Food & Nutrition Research, 54(1), 5144. https://doi.org/10.3402/fnr.v54i0.5144
Baulande, S., Lasnier, F., Lucas, M., & Pairault, J. (2001). Adiponutrin, a transmembrane protein corresponding to a novel dietary- and obesity-linked mRNA specifically expressed in the adipose lineage. The Journal of Biological Chemistry, 276(36), 33336–33344. https://doi.org/10.1074/jbc.M105193200
Bessard, T., Schutz, Y., & Jéquier, E. (1983). Energy expenditure and postprandial thermogenesis in obese women before and after weight loss. The American Journal of Clinical Nutrition, 38(5), 680–693. https://doi.org/10.1093/ajcn/38.5.680
Browne, G. J., & Proud, C. G. (2002). Regulation of peptide-chain elongation in mammalian cells. European Journal of Biochemistry, 269(22), 5360–5368.
Bryner, R. W., Ullrich, I. H., Sauers, J., Donley, D., Hornsby, G., Kolar, M., & Yeater, R. (1999). Effects of resistance vs. aerobic training combined with an 800 calorie liquid diet on lean body mass and resting metabolic rate. Journal of the American College of Nutrition, 18(2), 115–121.
Buchholz, A. C., & Schoeller, D. A. (2004). Is a calorie a calorie? The American Journal of Clinical Nutrition, 79(5), 899S-906S. https://doi.org/10.1093/ajcn/79.5.899S
Calbet, J. A. L., Ponce-González, J. G., Pérez-Suárez, I., La Calle Herrero, J. de, & Holmberg, H.-C. (2015). A time-efficient reduction of fat mass in 4 days with exercise and caloric restriction. Scandinavian Journal of Medicine & Science in Sports, 25(2), 223–233. https://doi.org/10.1111/sms.12194
Calbet, J. A. L., Ponce-González, J. G., La Calle-Herrero, J. d., Perez-Suarez, I., Martin-Rincon, M., Santana, A., . . . Holmberg, H.-C. (2017). Exercise Preserves Lean Mass and Performance during Severe Energy Deficit: The Role of Exercise Volume and Dietary Protein Content. Frontiers in Physiology, 8, 483. https://doi.org/10.3389/fphys.2017.00483
Campbell, P. J., Carlson, M. G., Hill, J. O., & Nurjhan, N. (1992). Regulation of free fatty acid metabolism by insulin in humans: Role of lipolysis and reesterification. The American Journal of Physiology, 263(6 Pt 1), E1063-9.
Camps, S. G. J. A., Verhoef, S. P. M., & Westerterp, K. R. (2013). Weight loss, weight maintenance, and adaptive thermogenesis. The American Journal of Clinical Nutrition, 97(5), 990–994. https://doi.org/10.3945/ajcn.112.050310
Carmen, G.-Y., & Víctor, S.-M. (2006). Signalling mechanisms regulating lipolysis. Cellular Signalling, 18(4), 401–408. https://doi.org/10.1016/j.cellsig.2005.08.009
Casanova, N., Beaulieu, K., Finlayson, G., & Hopkins, M. (2019). Metabolic adaptations during negative energy balance and their potential impact on appetite and food intake. The Proceedings of the Nutrition Society, 78(3), 279–289. https://doi.org/10.1017/S0029665118002811
Chaput, J.-P. (2010). Short sleep duration promoting overconsumption of food: A reward-driven eating behavior? Sleep, 33(9), 1135–1136. https://doi.org/10.1093/sleep/33.9.1135
Cummings, D. E., Frayo, R. S., Marmonier, C., Aubert, R., & Chapelot, D. (2004). Plasma ghrelin levels and hunger scores in humans initiating meals voluntarily without time- and food-related cues. American Journal of Physiology-Endocrinology and Metabolism, 287(2), E297-304. https://doi.org/10.1152/ajpendo.00582.2003
Cunningham, J. J. (1980). A reanalysis of the factors influencing basal metabolic rate in normal adults. The American Journal of Clinical Nutrition, 33(11), 2372–2374.
Dashti, H. S., Scheer, F. A., Jacques, P. F., Lamon-Fava, S., & Ordovás, J. M. (2015). Short sleep duration and dietary intake: Epidemiologic evidence, mechanisms, and health implications. Advances in Nutrition (Bethesda, Md.), 6(6), 648–659. https://doi.org/10.3945/an.115.008623
Donnelly, J. E., Jakicic, J., & Gunderson, S. (1991). Diet and body composition. Effect of very low calorie diets and exercise. Sports Medicine (Auckland, N.Z.), 12(4), 237–249. https://doi.org/10.2165/00007256-199112040-00003
Donnelly, J. E., Blair, S. N., Jakicic, J. M., Manore, M. M., Rankin, J. W., & Smith, B. K. (2009). American College of Sports Medicine Position Stand. Appropriate physical activity intervention strategies for weight loss and prevention of weight regain for adults. Medicine and Science in Sports and Exercise, 41(2), 459–471. https://doi.org/10.1249/MSS.0b013e3181949333
Drummen, M., Tischmann, L., Gatta-Cherifi, B., Fogelholm, M., Raben, A., Adam, T. C., & Westerterp-Plantenga, M. S. (2019). High Compared with Moderate Protein Intake Reduces Adaptive Thermogenesis and Induces a Negative Energy Balance during Long-term Weight-Loss Maintenance in Participants with Prediabetes in the Postobese State: A PREVIEW Study. The Journal of Nutrition. Advance online publication. https://doi.org/10.1093/jn/nxz281
Duncan, R. E., Ahmadian, M., Jaworski, K., Sarkadi-Nagy, E., & Sul, H. S. (2007). Regulation of lipolysis in adipocytes. Annual Review of Nutrition, 27, 79–101. https://doi.org/10.1146/annurev.nutr.27.061406.093734
Ebbeling, C. B., Feldman, H. A., Klein, G. L., Wong, J. M. W., Bielak, L., Steltz, S. K., . . . Ludwig, D. S. (2018). Effects of a low carbohydrate diet on energy expenditure during weight loss maintenance: Randomized trial. BMJ (Clinical Research Ed.), 363, k4583. https://doi.org/10.1136/bmj.k4583
Engeroff, T., Berk, D., Stücher, K., & Banzer, W. (2018). Resting metabolic rate – the applicability of predictive equations as an alternative to indirect calorimetry. Deutsche Zeitschrift für Sportmedizin, 2018(10), 319–325. https://doi.org/10.5960/dzsm.2018.348
Fagerberg, P. (2018). Negative Consequences of Low Energy Availability in Natural Male Bodybuilding: A Review. International Journal of Sport Nutrition and Exercise Metabolism, 28(4), 385–402. https://doi.org/10.1123/ijsnem.2016-0332
Flatt, J. P. (2007). Exaggerated claim about adaptive thermogenesis. International Journal of Obesity (2005), 31(10), 1626; author reply 1627-8. https://doi.org/10.1038/sj.ijo.0803641
Fogelholm, M. (1994). Effects of bodyweight reduction on sports performance. Sports Medicine (Auckland, N.Z.), 18(4), 249–267. https://doi.org/10.2165/00007256-199418040-00004
Forbes, G. B. (2000). Body fat content influences the body composition response to nutrition and exercise. Annals of the New York Academy of Sciences, 904, 359–365.
Furrer, R., & Handschin, C. (2020). Lifestyle vs. pharmacological interventions for healthy aging. Aging, 12(1), 5–7. https://doi.org/10.18632/aging.102741
Gallagher, D., Kovera, A. J., Clay-Williams, G., Agin, D., Leone, P., Albu, J., . . . Heymsfield, S. B. (2000). Weight loss in postmenopausal obesity: No adverse alterations in body composition and protein metabolism. American Journal of Physiology. Endocrinology and Metabolism, 279(1), E124-31. https://doi.org/10.1152/ajpendo.2000.279.1.E124
Gallagher, D., Kelley, D. E., Thornton, J., Boxt, L., Pi-Sunyer, X., Lipkin, E., . . . Heshka, S. (2017). Changes in skeletal muscle and organ size after a weight-loss intervention in overweight and obese type 2 diabetic patients. The American Journal of Clinical Nutrition, 105(1), 78–84. https://doi.org/10.3945/ajcn.116.139188
Gardner, C. D., Trepanowski, J. F., Del Gobbo, L. C., Hauser, M. E., Rigdon, J., Ioannidis, J. P. A., . . . King, A. C. (2018). Effect of Low-Fat vs Low-Carbohydrate Diet on 12-Month Weight Loss in Overweight Adults and the Association With Genotype Pattern or Insulin Secretion: The DIETFITS Randomized Clinical Trial. JAMA, 319(7), 667–679. https://doi.org/10.1001/jama.2018.0245
Garthe, I., Raastad, T., Refsnes, P. E., Koivisto, A., & Sundgot-Borgen, J. (2011). Effect of two different weight-loss rates on body composition and strength and power-related performance in elite athletes. International Journal of Sport Nutrition and Exercise Metabolism, 21(2), 97–104.
Gurvich, C., Hoy, K., Thomas, N., & Kulkarni, J. (2018). Sex Differences and the Influence of Sex Hormones on Cognition through Adulthood and the Aging Process. Brain Sciences, 8(9). https://doi.org/10.3390/brainsci8090163
Haaf, T. ten, & Weijs, P. J. M. (2014). Resting energy expenditure prediction in recreational athletes of 18-35 years: Confirmation of Cunningham equation and an improved weight-based alternative. PloS One, 9(9), e108460. https://doi.org/10.1371/journal.pone.0108460
Hall, K. D. (2008). What is the required energy deficit per unit weight loss? International Journal of Obesity (2005), 32(3), 573–576. https://doi.org/10.1038/sj.ijo.0803720
Hall, K. D. (2017). A review of the carbohydrate-insulin model of obesity. European Journal of Clinical Nutrition, 71(3), 323–326. https://doi.org/10.1038/ejcn.2016.260
Hall, K. D., & Guo, J. (2017). Obesity Energetics: Body Weight Regulation and the Effects of Diet Composition. Gastroenterology, 152(7), 1718-1727.e3. https://doi.org/10.1053/j.gastro.2017.01.052
Hall, K. D., Heymsfield, S. B., Kemnitz, J. W., Klein, S., SCHOELLER, D. A., & Speakman, J. R. (2012). Energy balance and its components: Implications for body weight regulation. The American Journal of Clinical Nutrition, 95(4), 989–994. https://doi.org/10.3945/ajcn.112.036350
Halton, T. L., & Hu, F. B. (2004). The effects of high protein diets on thermogenesis, satiety and weight loss: A critical review. Journal of the American College of Nutrition, 23(5), 373–385.
Heikura, I. A., Uusitalo, A. L. T., Stellingwerff, T., Bergland, D., Mero, A. A., & Burke, L. M. (2018). Low Energy Availability Is Difficult to Assess but Outcomes Have Large Impact on Bone Injury Rates in Elite Distance Athletes. International Journal of Sport Nutrition and Exercise Metabolism, 28(4), 403–411. https://doi.org/10.1123/ijsnem.2017-0313
Heymsfield, S. B., Thomas, D., Nguyen, A. M., Peng, J. Z., Martin, C., Shen, W., . . . Muller, M. J. (2011). Voluntary weight loss: Systematic review of early phase body composition changes. Obesity Reviews : an Official Journal of the International Association for the Study of Obesity, 12(5), e348-61. https://doi.org/10.1111/j.1467-789X.2010.00767.x
Hooper, L., Abdelhamid, A., Moore, H. J., Douthwaite, W., Skeaff, C. M., & Summerbell, C. D. (2012). Effect of reducing total fat intake on body weight: Systematic review and meta-analysis of randomised controlled trials and cohort studies. BMJ (Clinical Research Ed.), 345, e7666. https://doi.org/10.1136/bmj.e7666
Howell, S., & Kones, R. (2017). „Calories in, calories out“ and macronutrient intake: The hope, hype, and science of calories. American Journal of Physiology. Endocrinology and Metabolism, 313(5), E608-E612. https://doi.org/10.1152/ajpendo.00156.2017
Jiang, Y., Tan, S., Wang, Z., Guo, Z., Li, Q., & Wang, J. (2020). Aerobic exercise training at maximal fat oxidation intensity improves body composition, glycemic control, and physical capacity in older people with type 2 diabetes. Journal of Exercise Science and Fitness, 18(1), 7–13. https://doi.org/10.1016/j.jesf.2019.08.003
Jlid, M. C., Maffulli, N., Elloumi, M., Moalla, W., & Paillard, T. (2013). Rapid weight loss alters muscular performance and perceived exertion as well as postural control in elite wrestlers. The Journal of Sports Medicine and Physical Fitness, 53(6), 620–627.
Jocken, J. W. E., & Blaak, E. E. (2008). Catecholamine-induced lipolysis in adipose tissue and skeletal muscle in obesity. Physiology & Behavior, 94(2), 219–230. https://doi.org/10.1016/j.physbeh.2008.01.002
Johnstone, A. M., Murison, S. D., Duncan, J. S., Rance, K. A., & Speakman, J. R. (2005). Factors influencing variation in basal metabolic rate include fat-free mass, fat mass, age, and circulating thyroxine but not sex, circulating leptin, or triiodothyronine. The American Journal of Clinical Nutrition, 82(5), 941–948. https://doi.org/10.1093/ajcn/82.5.941
Kaiyala, K. J., & Ramsay, D. S. (2011). Direct animal calorimetry, the underused gold standard for quantifying the fire of life. Comparative Biochemistry and Physiology. Part A, Molecular & Integrative Physiology, 158(3), 252–264. https://doi.org/10.1016/j.cbpa.2010.04.013
Karila, T. A. M., Sarkkinen, P., Marttinen, M., Seppälä, T., Mero, A., & Tallroth, K. (2008). Rapid weight loss decreases serum testosterone. International Journal of Sports Medicine, 29(11), 872–877. https://doi.org/10.1055/s-2008-1038604
Kistler, B. M., Fitschen, P. J., Ranadive, S. M., Fernhall, B., & Wilund, K. R. (2014). Case study: Natural bodybuilding contest preparation. International Journal of Sport Nutrition and Exercise Metabolism, 24(6), 694–700. https://doi.org/10.1123/ijsnem.2014-0016
Large, V., Peroni, O., Letexier, D., Ray, H., & Beylot, M. (2004). Metabolism of lipids in human white adipocyte. Diabetes & Metabolism, 30(4), 294–309.
Leckey, J. J., Hoffman, N. J., Parr, E. B., Devlin, B. L., Trewin, A. J., Stepto, N. K., . . . Hawley, J. A. (2018). High dietary fat intake increases fat oxidation and reduces skeletal muscle mitochondrial respiration in trained humans. FASEB Journal : Official Publication of the Federation of American Societies for Experimental Biology, 32(6), 2979–2991. https://doi.org/10.1096/fj.201700993R
Levine, D. I. (2017). The Curious History of the Calorie in U.S. Policy: : A Tradition of Unfulfilled Promises. American Journal of Preventive Medicine, 52(1), 125–129. https://doi.org/10.1016/j.amepre.2016.08.012
Levine, J. A. (2007). Nonexercise activity thermogenesis ? Liberating the life-force. Journal of Internal Medicine, 262(3), 273–287. https://doi.org/10.1111/j.1365-2796.2007.01842.x
Levine, J. A. (2004). Nonexercise activity thermogenesis (NEAT): Environment and biology. American Journal of Physiology-Endocrinology and Metabolism, 286(5), E675-E685. https://doi.org/10.1152/ajpendo.00562.2003
Lichtman, S. W., Pisarska, K., Berman, E. R., Pestone, M., Dowling, H., Offenbacher, E., . . . Heymsfield, S. B. (1992). Discrepancy between self-reported and actual caloric intake and exercise in obese subjects. The New England Journal of Medicine, 327(27), 1893–1898. https://doi.org/10.1056/NEJM199212313272701
Feingold, K. R., Anawalt, B., Boyce, A., Chrousos, G., Dungan, K., Grossman, A.,. . . Wilson, D. P. (Eds.) (2000). Endotext: The Role of Non-exercise Activity Thermogenesis in Human Obesity. South Dartmouth (MA).
Loucks, A. B. (2004). Energy balance and body composition in sports and exercise. Journal of Sports Sciences, 22(1), 1–14. https://doi.org/10.1080/0264041031000140518
Ludwig, D. S. (2002). The glycemic index: Physiological mechanisms relating to obesity, diabetes, and cardiovascular disease. JAMA, 287(18), 2414–2423. https://doi.org/10.1001/jama.287.18.2414
Ludwig, D. S., & Ebbeling, C. B. (2018). The Carbohydrate-Insulin Model of Obesity: Beyond „Calories In, Calories Out“. JAMA Internal Medicine, 178(8), 1098–1103. https://doi.org/10.1001/jamainternmed.2018.2933
Ludwig, D. S., & Friedman, M. I. (2014). Increasing adiposity: Consequence or cause of overeating? JAMA, 311(21), 2167–2168. https://doi.org/10.1001/jama.2014.4133
Ludwig, D. S., Lakin, P. R., Wong, W. W., & Ebbeling, C. B. (2019). Scientific discourse in the era of open science: A response to Hall et al. regarding the Carbohydrate-Insulin Model. International Journal of Obesity (2005), 43(12), 2355–2360. https://doi.org/10.1038/s41366-019-0466-1
Maclean, P. S., Blundell, J. E., Mennella, J. A., & Batterham, R. L. (2017). Biological control of appetite: A daunting complexity. Obesity (Silver Spring, Md.), 25 Suppl 1, S8-S16. https://doi.org/10.1002/oby.21771
Mansoor, N., Vinknes, K. J., Veierød, M. B., & Retterstøl, K. (2016). Effects of low-carbohydrate diets v. low-fat diets on body weight and cardiovascular risk factors: A meta-analysis of randomised controlled trials. The British Journal of Nutrition, 115(3), 466–479. https://doi.org/10.1017/S0007114515004699
Margolis, L. M., Rivas, D. A., Berrone, M., Ezzyat, Y., Young, A. J., McClung, J. P., . . . Pasiakos, S. M. (2016). Prolonged Calorie Restriction Downregulates Skeletal Muscle mTORC1 Signaling Independent of Dietary Protein Intake and Associated microRNA Expression. Frontiers in Physiology, 7, 445. https://doi.org/10.3389/fphys.2016.00445
Miles, C. W., Kelsay, J. L., & Wong, N. P. (1988). Effect of dietary fiber on the metabolizable energy of human diets. The Journal of Nutrition, 118(9), 1075–1081. https://doi.org/10.1093/jn/118.9.1075
Minichowski, D. (2020). Cardio, Diät & Muskelaufbau: Der Interferenz-Effekt. Aesirsports. Retrieved from https://aesirsports.de/cardio-interferenz-diaet-muskelaufbau/
Moe, P. W. (1994). Future directions for energy requirements and food energy values. The Journal of Nutrition, 124(9 Suppl), 1738S-1742S. https://doi.org/10.1093/jn/124.suppl_9.1738S
Mountjoy, M., Sundgot-Borgen, J. K., Burke, L. M., Ackerman, K. E., Blauwet, C., Constantini, N., . . . Budgett, R. (2018). IOC consensus statement on relative energy deficiency in sport (RED-S): 2018 update. British Journal of Sports Medicine, 52(11), 687–697. https://doi.org/10.1136/bjsports-2018-099193
Mountjoy, M., Sundgot-Borgen, J., Burke, L., Carter, S., Constantini, N., Lebrun, C., . . . Ljungqvist, A. (2014). The IOC consensus statement: Beyond the Female Athlete Triad–Relative Energy Deficiency in Sport (RED-S). British Journal of Sports Medicine, 48(7), 491–497. https://doi.org/10.1136/bjsports-2014-093502
Müller, M. J., Enderle, J., & Bosy-Westphal, A. (2016). Changes in Energy Expenditure with Weight Gain and Weight Loss in Humans. Current Obesity Reports, 5(4), 413–423. https://doi.org/10.1007/s13679-016-0237-4
Müller, M. J., & Bosy-Westphal, A. (2019). Effect of Over- and Underfeeding on Body Composition and Related Metabolic Functions in Humans. Current Diabetes Reports, 19(11), 108. https://doi.org/10.1007/s11892-019-1221-7
Müller, M. J., Enderle, J., Pourhassan, M., Braun, W., Eggeling, B., Lagerpusch, M., . . . Bosy-Westphal, A. (2015). Metabolic adaptation to caloric restriction and subsequent refeeding: The Minnesota Starvation Experiment revisited. The American Journal of Clinical Nutrition, 102(4), 807–819. https://doi.org/10.3945/ajcn.115.109173
Murphy, C., & Koehler, K. (2020). Caloric restriction induces anabolic resistance to resistance exercise. European Journal of Applied Physiology. Advance online publication. https://doi.org/10.1007/s00421-020-04354-0
National Academies Press (US) (2017). Nutrition Across the Lifespan for Healthy Aging: Proceedings of a Workshop. Washington (DC).
Nattiv, A., Loucks, A. B., Manore, M. M., Sanborn, C. F., Sundgot-Borgen, J., & Warren, M. P. (2007). American College of Sports Medicine position stand. The female athlete triad. Medicine and Science in Sports and Exercise, 39(10), 1867–1882. https://doi.org/10.1249/mss.0b013e318149f111
Nicklas, B. J., Chmelo, E., Delbono, O., Carr, J. J., Lyles, M. F., & Marsh, A. P. (2015). Effects of resistance training with and without caloric restriction on physical function and mobility in overweight and obese older adults: A randomized controlled trial. The American Journal of Clinical Nutrition, 101(5), 991–999. https://doi.org/10.3945/ajcn.114.105270
Pasiakos, S. M., Cao, J. J., Margolis, L. M., Sauter, E. R., Whigham, L. D., McClung, J. P., . . . Young, A. J. (2013). Effects of high-protein diets on fat-free mass and muscle protein synthesis following weight loss: A randomized controlled trial. FASEB Journal : Official Publication of the Federation of American Societies for Experimental Biology, 27(9), 3837–3847. https://doi.org/10.1096/fj.13-230227
Pasiakos, S. M., Vislocky, L. M., Carbone, J. W., Altieri, N., Konopelski, K., Freake, H. C., . . . Rodriguez, N. R. (2010). Acute energy deprivation affects skeletal muscle protein synthesis and associated intracellular signaling proteins in physically active adults. The Journal of Nutrition, 140(4), 745–751. https://doi.org/10.3945/jn.109.118372
Perea, A., Clemente, F., Martinell, J., Villanueva-Peñacarrillo, M. L., & Valverde, I. (1995). Physiological effect of glucagon in human isolated adipocytes. Hormone and Metabolic Research = Hormon- Und Stoffwechselforschung = Hormones Et Metabolisme, 27(8), 372–375. https://doi.org/10.1055/s-2007-979981
Perry, B., & Wang, Y. (2012). Appetite regulation and weight control: The role of gut hormones. Nutrition & Diabetes, 2, e26. https://doi.org/10.1038/nutd.2011.21
Petrizzo, J., DiMenna, F. J., Martins, K., Wygand, J., & Otto, R. M. (2017). Case Study: The Effect of 32 Weeks of Figure-Contest Preparation on a Self-Proclaimed Drug-Free Female’s Lean Body and Bone Mass. International Journal of Sport Nutrition and Exercise Metabolism, 27(6), 543–549. https://doi.org/10.1123/ijsnem.2016-0313
Racette, S. B., Schoeller, D. A., Kushner, R. F., Neil, K. M., & Herling-Iaffaldano, K. (1995). Effects of aerobic exercise and dietary carbohydrate on energy expenditure and body composition during weight reduction in obese women. The American Journal of Clinical Nutrition, 61(3), 486–494. https://doi.org/10.1093/ajcn/61.3.486
Ragolia, L., & Begum, N. (1998). Protein phosphatase-1 and insulin action. Molecular and Cellular Biochemistry, 182(1-2), 49–58.
Rankin, J. W. (2002). Weight loss and gain in athletes. Current Sports Medicine Reports, 1(4), 208–213.
Ravussin, E., & Bogardus, C. (1989). Relationship of genetics, age, and physical fitness to daily energy expenditure and fuel utilization. The American Journal of Clinical Nutrition, 49(5 Suppl), 968–975. https://doi.org/10.1093/ajcn/49.5.968
Ravussin, E., Schutz, Y., Acheson, K. J., Dusmet, M., Bourquin, L., & Jéquier, E. (1985). Short-term, mixed-diet overfeeding in man: No evidence for „luxuskonsumption“. The American Journal of Physiology, 249(5 Pt 1), E470-7. https://doi.org/10.1152/ajpendo.1985.249.5.E470
Robinson, S. L., Lambeth-Mansell, A., Gillibrand, G., Smith-Ryan, A., & Bannock, L. (2015). A nutrition and conditioning intervention for natural bodybuilding contest preparation: Case study. Journal of the International Society of Sports Nutrition, 12, 20. https://doi.org/10.1186/s12970-015-0083-x
Rohrig, B. J., Pettitt, R. W., Pettitt, C. D., & Kanzenbach, T. L. (2017). Psychophysiological Tracking of a Female Physique Competitor through Competition Preparation. International Journal of Exercise Science, 10(2), 301–311.
Rosa-Caldwell, M. E., & Greene, N. P. (2019). Muscle metabolism and atrophy: Let’s talk about sex. Biology of Sex Differences, 10(1), 43. https://doi.org/10.1186/s13293-019-0257-3
Rosenbaum, M., Vandenborne, K., Goldsmith, R., Simoneau, J.-A., Heymsfield, S., Joanisse, D. R., . . . Leibel, R. L. (2003). Effects of experimental weight perturbation on skeletal muscle work efficiency in human subjects. American Journal of Physiology. Regulatory, Integrative and Comparative Physiology, 285(1), R183-92. https://doi.org/10.1152/ajpregu.00474.2002
Roth, C., Rettenmaier, L., & Behringer, M. (2020). High-Protein Energy-Restriction (30kcal/kg), Lean Mass Retention, Contractile Properties and Mood in College Athletes. Unveröffentlichtes Manuskript.
Sainsbury, A., & Zhang, L. (2010). Role of the arcuate nucleus of the hypothalamus in regulation of body weight during energy deficit. Molecular and Cellular Endocrinology, 316(2), 109–119. https://doi.org/10.1016/j.mce.2009.09.025
Schwartz, M. W., Seeley, R. J., Zeltser, L. M., Drewnowski, A., Ravussin, E., Redman, L. M., & Leibel, R. L. (2017). Obesity Pathogenesis: An Endocrine Society Scientific Statement. Endocrine Reviews, 38(4), 267–296. https://doi.org/10.1210/er.2017-00111
Seaton, T. B., Welle, S. L., Warenko, M. K., & Campbell, R. G. (1986). Thermic effect of medium-chain and long-chain triglycerides in man. The American journal of clinical nutrition, 44(5), 630–634. https://doi.org/10.1093/ajcn/44.5.630
Seimon, R. V., Wild-Taylor, A. L., Keating, S. E., McClintock, S., Harper, C., Gibson, A. A., . . . Sainsbury, A. (2019). Effect of Weight Loss via Severe vs Moderate Energy Restriction on Lean Mass and Body Composition Among Postmenopausal Women With Obesity: The TEMPO Diet Randomized Clinical Trial. JAMA Network Open, 2(10), e1913733. https://doi.org/10.1001/jamanetworkopen.2019.13733
Silbernagl, S., & Despopoulos, A. (2012). Taschenatlas Physiologie (8. überarb. u. erw. Aufl.). Stuttgart u.a.: Thieme.
Silva, A. M., Júdice, P. B., Carraça, E. V., King, N., Teixeira, P. J., & Sardinha, L. B. (2018). What is the effect of diet and/or exercise interventions on behavioural compensation in non-exercise physical activity and related energy expenditure of free-living adults? A systematic review. The British Journal of Nutrition, 119(12), 1327–1345. https://doi.org/10.1017/S000711451800096X
Siw Eriksson, L., Olsson, M., & Björkman, O. (1988). Splanchnic metabolism of amino acids in healthy subjects: Effect of 60 hours of fasting. Metabolism, 37(12), 1159–1162. https://doi.org/10.1016/0026-0495(88)90194-1
Smiles, W. J., Areta, J. L., Coffey, V. G., Phillips, S. M., Moore, D. R., Stellingwerff, T., . . . Camera, D. M. (2015). Modulation of autophagy signaling with resistance exercise and protein ingestion following short-term energy deficit. American Journal of Physiology. Regulatory, Integrative and Comparative Physiology, 309(5), R603-12. https://doi.org/10.1152/ajpregu.00413.2014
Spriet, L. L. (2014). New insights into the interaction of carbohydrate and fat metabolism during exercise. Sports Medicine (Auckland, N.Z.), 44 Suppl 1, S87-96. https://doi.org/10.1007/s40279-014-0154-1
Stapley, L. (2001). Sex differences are more than just hormonal. Trends in Endocrinology & Metabolism, 12(5), 190. https://doi.org/10.1016/S1043-2760(01)00419-2
Stellingwerff, T., & Cox, G. R. (2014). Systematic review: Carbohydrate supplementation on exercise performance or capacity of varying durations. Applied Physiology, Nutrition, and Metabolism = Physiologie Appliquee, Nutrition Et Metabolisme, 39(9), 998–1011. https://doi.org/10.1139/apnm-2014-0027
Stubbs, R. J., Hopkins, M., Finlayson, G. S., Duarte, C., Gibbons, C., & Blundell, J. E. (2018). Potential effects of fat mass and fat-free mass on energy intake in different states of energy balance. European journal of clinical nutrition, 72(5), 698–709. https://doi.org/10.1038/s41430-018-0146-6
Sumithran, P., Prendergast, L. A., Delbridge, E., Purcell, K., Shulkes, A., Kriketos, A., & Proietto, J. (2011). Long-term persistence of hormonal adaptations to weight loss. The New England Journal of Medicine, 365(17), 1597–1604. https://doi.org/10.1056/NEJMoa1105816
Taeger, F. (2018). Satt, Stark, Schlank: Ernährungsstrategien für Performance und Gesundheit. Pulheim: Eigenverlag.
Tinsley, G. M., Trexler, E. T., Smith-Ryan, A. E., Paoli, A., Graybeal, A. J., Campbell, B. I., & Schoenfeld, B. J. (2018). Changes in Body Composition and Neuromuscular Performance Through Preparation, 2 Competitions, and a Recovery Period in an Experienced Female Physique Athlete. Journal of Strength and Conditioning Research. Advance online publication. https://doi.org/10.1519/JSC.0000000000002758
Torbay, N., Bracco, E. F., Geliebter, A., Stewart, I. M., & Hashim, S. A. (1985). Insulin increases body fat despite control of food intake and physical activity. The American Journal of Physiology, 248(1 Pt 2), R120-4. https://doi.org/10.1152/ajpregu.1985.248.1.R120
Tremblay, A., Royer, M.-M., Chaput, J.-P., & Doucet, E. (2013). Adaptive thermogenesis can make a difference in the ability of obese individuals to lose body weight. International Journal of Obesity (2005), 37(6), 759–764. https://doi.org/10.1038/ijo.2012.124
Trexler, E. T., Smith-Ryan, A. E., & Norton, L. E. (2014). Metabolic adaptation to weight loss: Implications for the athlete. Journal of the International Society of Sports Nutrition, 11(1), 7. https://doi.org/10.1186/1550-2783-11-7
Velasquez-Mieyer, P. A., Cowan, P. A., Arheart, K. L., Buffington, C. K., Spencer, K. A., Connelly, B. E., . . . Lustig, R. H. (2003). Suppression of insulin secretion is associated with weight loss and altered macronutrient intake and preference in a subset of obese adults. International Journal of Obesity and Related Metabolic Disorders : Journal of the International Association for the Study of Obesity, 27(2), 219–226. https://doi.org/10.1038/sj.ijo.802227
Villena, J. A., Roy, S., Sarkadi-Nagy, E., Kim, K.-H., & Sul, H. S. (2004). Desnutrin, an adipocyte gene encoding a novel patatin domain-containing protein, is induced by fasting and glucocorticoids: Ectopic expression of desnutrin increases triglyceride hydrolysis. The Journal of Biological Chemistry, 279(45), 47066–47075. https://doi.org/10.1074/jbc.M403855200
Watt, M. J., Krustrup, P., Secher, N. H., Saltin, B., Pedersen, B. K., & Febbraio, M. A. (2004). Glucose ingestion blunts hormone-sensitive lipase activity in contracting human skeletal muscle. American Journal of Physiology. Endocrinology and Metabolism, 286(1), E144-50. https://doi.org/10.1152/ajpendo.00198.2003
Weck, M., Bornstein, S. R., Barthel, A., & Blüher, M. (2012). Wie ist Gewichtsreduktion erfolgreich möglich? [Strategies for successful weight reduction – focus on energy balance]. Deutsche medizinische Wochenschrift (1946), 137(43), 2223–2228. https://doi.org/10.1055/s-0032-1327232
Weigle, D. S. (1988). Contribution of decreased body mass to diminished thermic effect of exercise in reduced-obese men. International Journal of Obesity, 12(6), 567–578.
Westerterp, K. R. (2013). Physical activity and physical activity induced energy expenditure in humans: Measurement, determinants, and effects. Frontiers in Physiology, 4, 90. https://doi.org/10.3389/fphys.2013.00090
Widdowsen, E. M. (1955). Assessment of the energy value of human foods. The Proceedings of the Nutrition Society, 14(2), 142–154. https://doi.org/10.1079/PNS19550031
Williams, T., Walz, E., Lane, A. R., Pebole, M., & Hackney, A. C. (2015). The effect of estrogen on muscle damage biomarkers following prolonged aerobic exercise in eumenorrheic women. Biology of Sport, 32(3), 193–198. https://doi.org/10.5604/20831862.1150300
Wilson, G., Hawken, M. B., Poole, I., Sparks, A., Bennett, S., Drust, B., . . . Close, G. L. (2014). Rapid weight-loss impairs simulated riding performance and strength in jockeys: Implications for making-weight. Journal of Sports Sciences, 32(4), 383–391. https://doi.org/10.1080/02640414.2013.825732
Witard, O. C., Garthe, I., & Phillips, S. M. (2019). Dietary Protein for Training Adaptation and Body Composition Manipulation in Track and Field Athletes. International Journal of Sport Nutrition and Exercise Metabolism, 29(2), 165–174. https://doi.org/10.1123/ijsnem.2018-0267
Zimmermann, R., Strauss, J. G., Haemmerle, G., Schoiswohl, G., Birner-Gruenberger, R., Riederer, M., . . . Zechner, R. (2004). Fat mobilization in adipose tissue is promoted by adipose triglyceride lipase. Science (New York, N.Y.), 306(5700), 1383–1386. https://doi.org/10.1126/science.1100747


Schreibe einen Kommentar